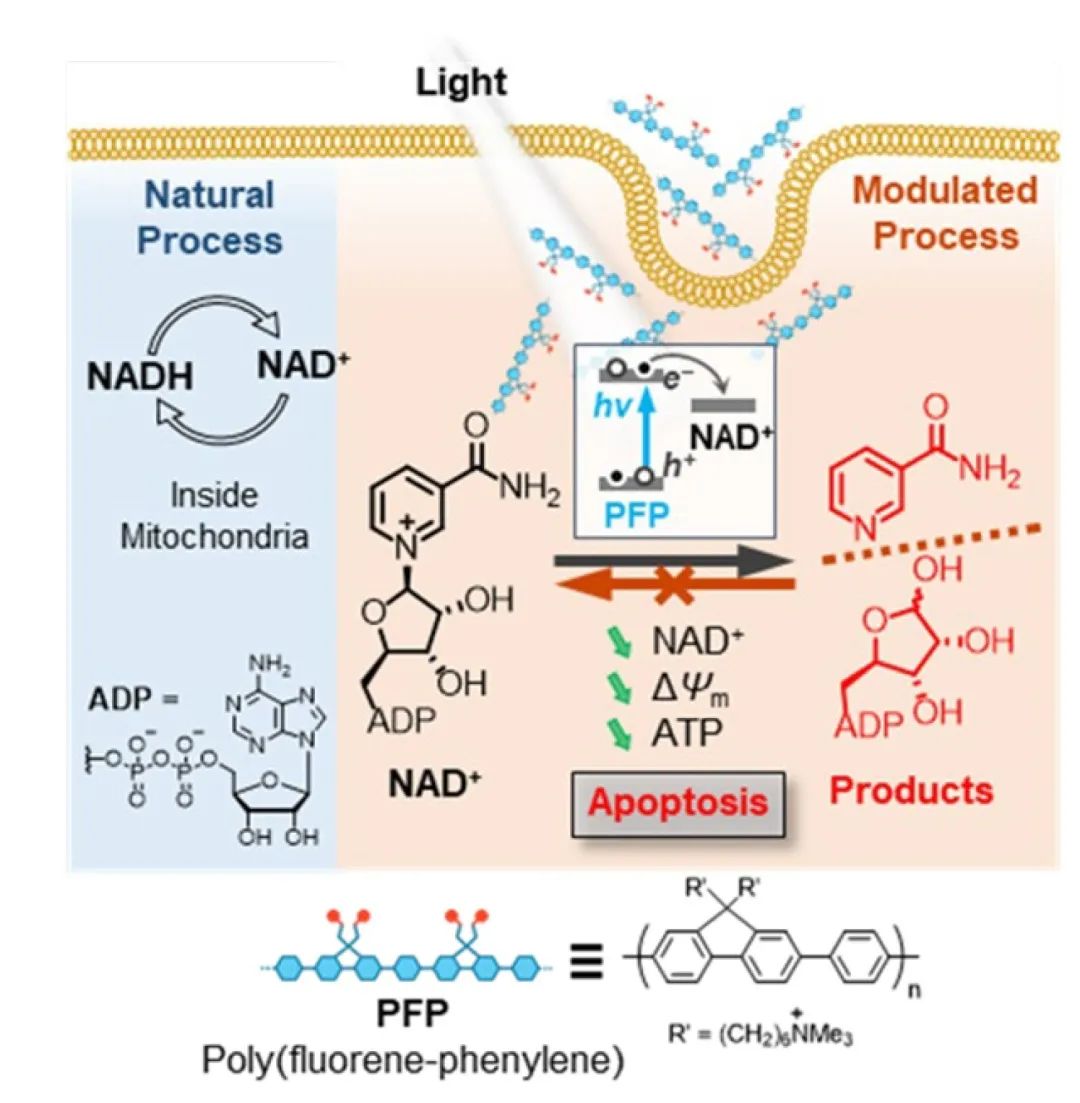
圖1. 細胞内光催化分(fēn)解NAD+的反應示意圖
生(shēng)物(wù)代謝是細胞生(shēng)命活動的基礎,決定了細胞正常的生(shēng)命活動和生(shēng)物(wù)功能。當細胞出現代謝紊亂時,其内部生(shēng)物(wù)功能會受到影響,甚至導緻疾病的發生(shēng)。NAD+/NADH是參與腫瘤代謝氧化還原反應的重要輔酶,在糖酵解、三羧酸循環(TCA)等代謝過程中(zhōng)發揮着重要作用。已有報道證實,通過化學反應将細胞内的NAD+還原爲NADH,能夠有效幹擾癌細胞的生(shēng)物(wù)功能,從而實現對癌細胞的殺傷。但由于細胞具有自我(wǒ)(wǒ)修複的特性,NAD+的還原容易被細胞其他代謝途徑恢複,因此難以打破腫瘤細胞内NAD+/NADH的動态平衡。同時,傳統化學反應需要滿足高溫、無水等苛刻的條件,這限制了它們在細胞内複雜(zá)生(shēng)理環境的應用。相比之下(xià),光催化反應具有反應條件溫和、便于遠程調控等優勢,這使得在細胞内NAD+轉化變得可行。水溶性共轭聚合物(wù)具有優異的光電(diàn)轉化能力、高效的電(diàn)子轉移效率和良好的生(shēng)物(wù)相容性,可作爲新型光催化劑,通過在細胞内進行光催化反應,實現對癌細胞代謝的調控,從而促使腫瘤細胞凋亡。
該工(gōng)作報道了一(yī)種以水溶性共轭聚合物(wù)PFP作爲催化劑的新型光催化反應,在常溫常壓下(xià)實現了NAD+的裂解(圖2)。在白(bái)光照射下(xià),作者将PFP用于無氧條件下(xià)水溶液體(tǐ)系中(zhōng)NAD+裂解反應,并對産物(wù)進行了表征和分(fēn)析。通過核磁共振和質譜技術确定了NAD+的裂解産物(wù)爲煙酰胺和ADP-核糖,并通過核磁共振氫譜定量分(fēn)析計算出光照1小(xiǎo)時後煙酰胺産物(wù)濃度達到113 μM。該反應在溫和無氧的水溶液體(tǐ)系中(zhōng)可以實現NAD+的裂解,而不是還原生(shēng)成NADH。這意味着該反應可以實現NAD+的不可逆轉化,并有可能調節乏氧腫瘤細胞内NAD+/NADH的動态平衡,抑制腫瘤細胞的生(shēng)長。
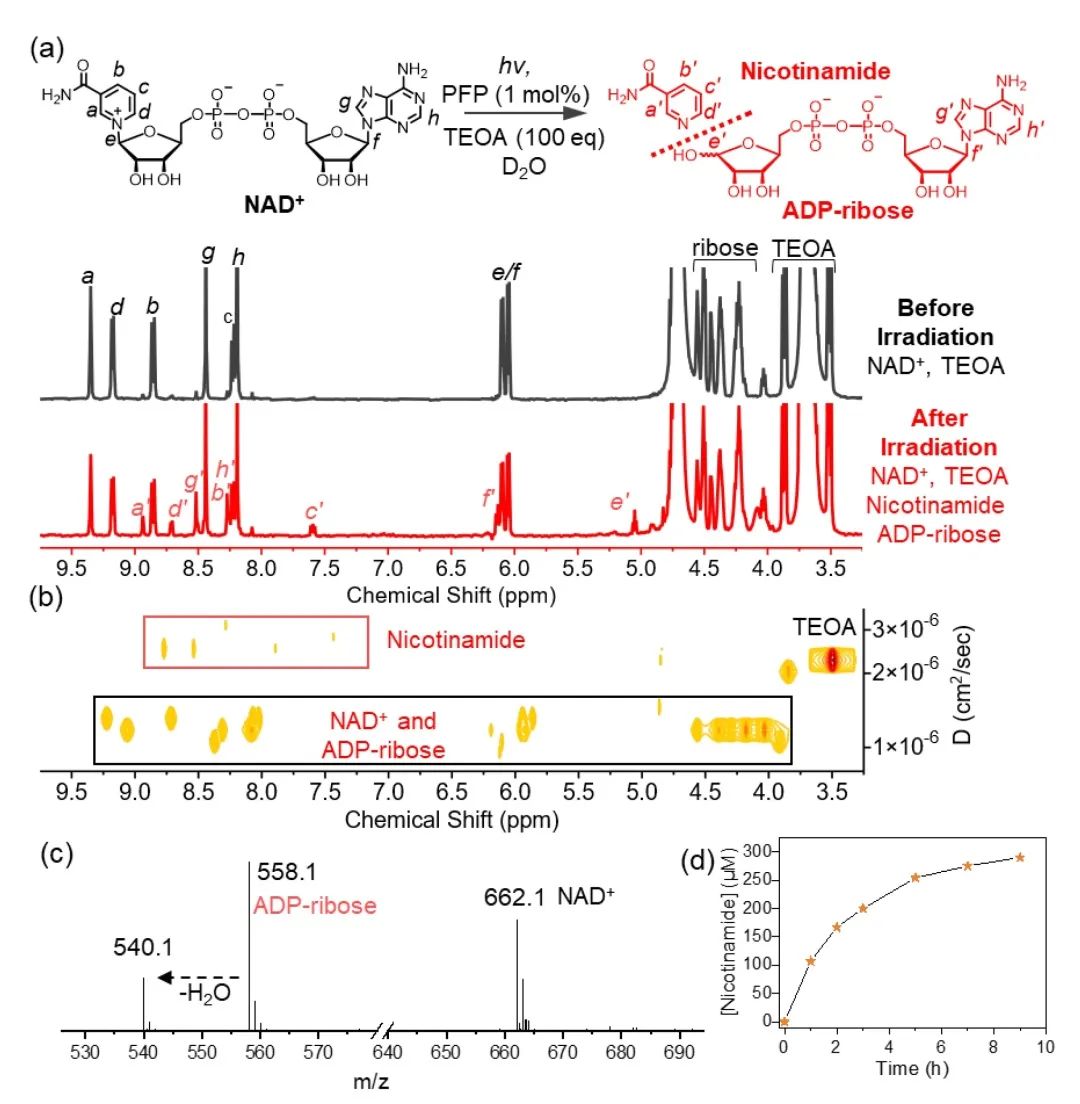
圖2. PFP光催化NAD+分(fēn)解。
随後,作者将該光催化反應體(tǐ)系引入乏氧處理的小(xiǎo)鼠乳腺癌細胞4T1中(zhōng)。實驗結果發現8 μM的 PFP共孵育的4T1細胞在光照20分(fēn)鍾後,細胞内NAD+比例從73%下(xià)降到65%,并出現明顯的細胞損傷。細胞線粒體(tǐ)膜電(diàn)位降低和ATP含量顯著下(xià)降都表明其線粒體(tǐ)電(diàn)子傳遞鏈受損(圖3)。這些數據表明該光催化反應可以在細胞内實現,并通過影響線粒體(tǐ)電(diàn)子傳遞鏈調控腫瘤細胞的凋亡。
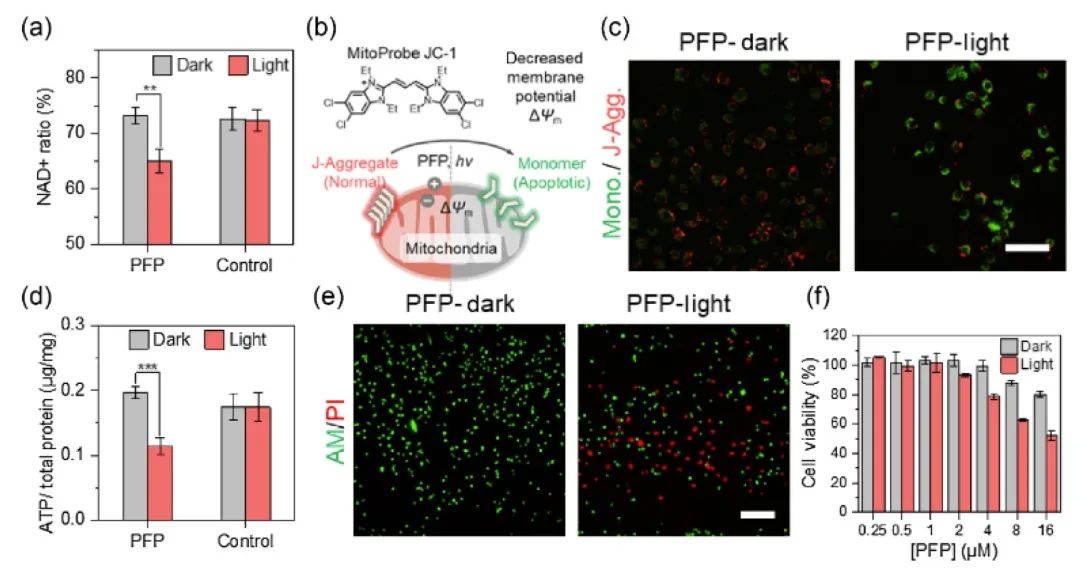
圖3. PFP在光照下(xià)促進癌細胞凋亡。
作者利用電(diàn)子順磁共振(EPR)進一(yī)步對光催化反應的機理進行了研究。光照條件下(xià),PFP和NAD+的混合物(wù)呈現碳自由基被捕獲的信号,結合已知(zhī)産物(wù)結構,推測PFP*與NAD+之間的電(diàn)子轉移産生(shēng)了ADP-ribosyl自由基,最終生(shēng)成穩定的産物(wù)ADP-核糖,實現NAD+的不可逆裂解反應。
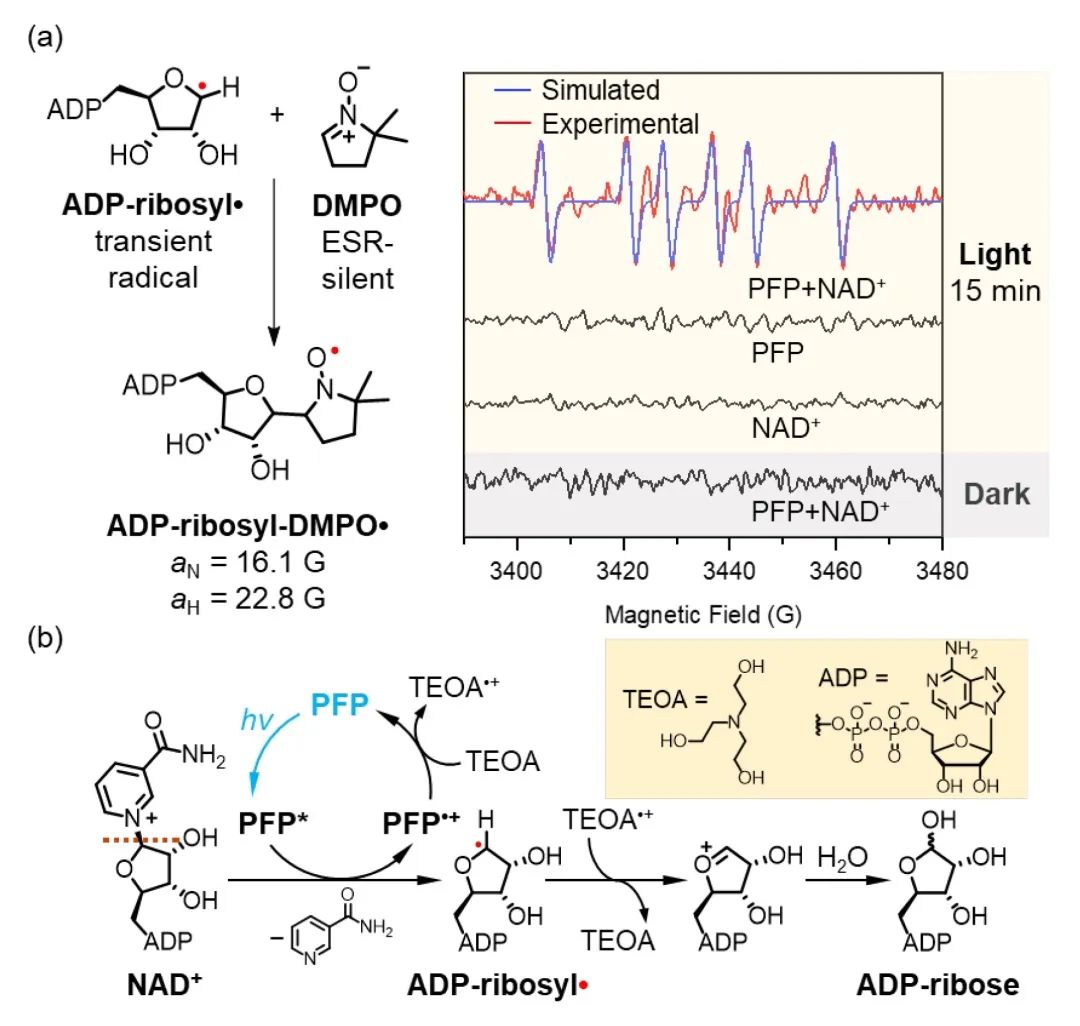
圖4. PFP光催化裂解NAD+的機理研究。
該工(gōng)作報道了一(yī)種以水溶性共轭聚合物(wù)作爲催化劑的新型光催化反應,在光照條件下(xià)将NAD+不可逆地裂解爲煙酰胺和ADP-核糖。細胞實驗證實,該反應可實現乏氧腫瘤細胞中(zhōng)NAD+的消耗,從而促進腫瘤細胞4T1凋亡。這項工(gōng)作利用化學手段實現了腫瘤細胞的代謝幹預,爲可控腫瘤細胞凋亡提供了一(yī)種新策略。
論文第一(yī)作者爲中(zhōng)國科學院化學研究所博士研究生(shēng)夏晟鵬,通訊作者爲王樹(shù)研究員(yuán)、白(bái)昊天研究員(yuán)和黃一(yī)鳴副研究員(yuán)。該研究得到了國家自然科學基金的大(dà)力支持。該工(gōng)作以研究論文(Research Article)形式發表在中(zhōng)國化學會旗艦期刊CCS Chemistry上。
文章詳情:
 掃一(yī)掃,關注微信
掃一(yī)掃,關注微信
技術支持:化工(gōng)儀器網 管理登陸
微信掃一(yī)掃
